所有文章
快速入门
操作视频中心
实名认证
合同起草协商
发起合同
合同审批
合同签署
相对方
合同管理
合同归档
合同审查
合同比对
组织管理
电子印章管理
合同费用管理
系统权限设置
企业用户使用手册
如何创建企业
如何进行企业认证
企业认证 操作路径图
选择企业身份进入工作台
签署
发起签署
如何使用本地文件发起合同
如何使用模板发起合同
如何查看可用的模板
如何批量发起签署任务
如何使用扫码签
收件人角色的参与方式有哪些
如何发起文件签署 NEW
如何由动态收件人自助(扫码)发起文件签署 ?
如何由动态收件人自助(扫码)发起文件签署 ?
如何批量发起文件签署 ?
如何批量发起不同文件签署 ?
如何批量导入收件组(或签) ?
如何批量导入图片字段 ?
如何批量导入表格字段 ?
如何设置文件水印 ?
如何设置保密件签署 ?
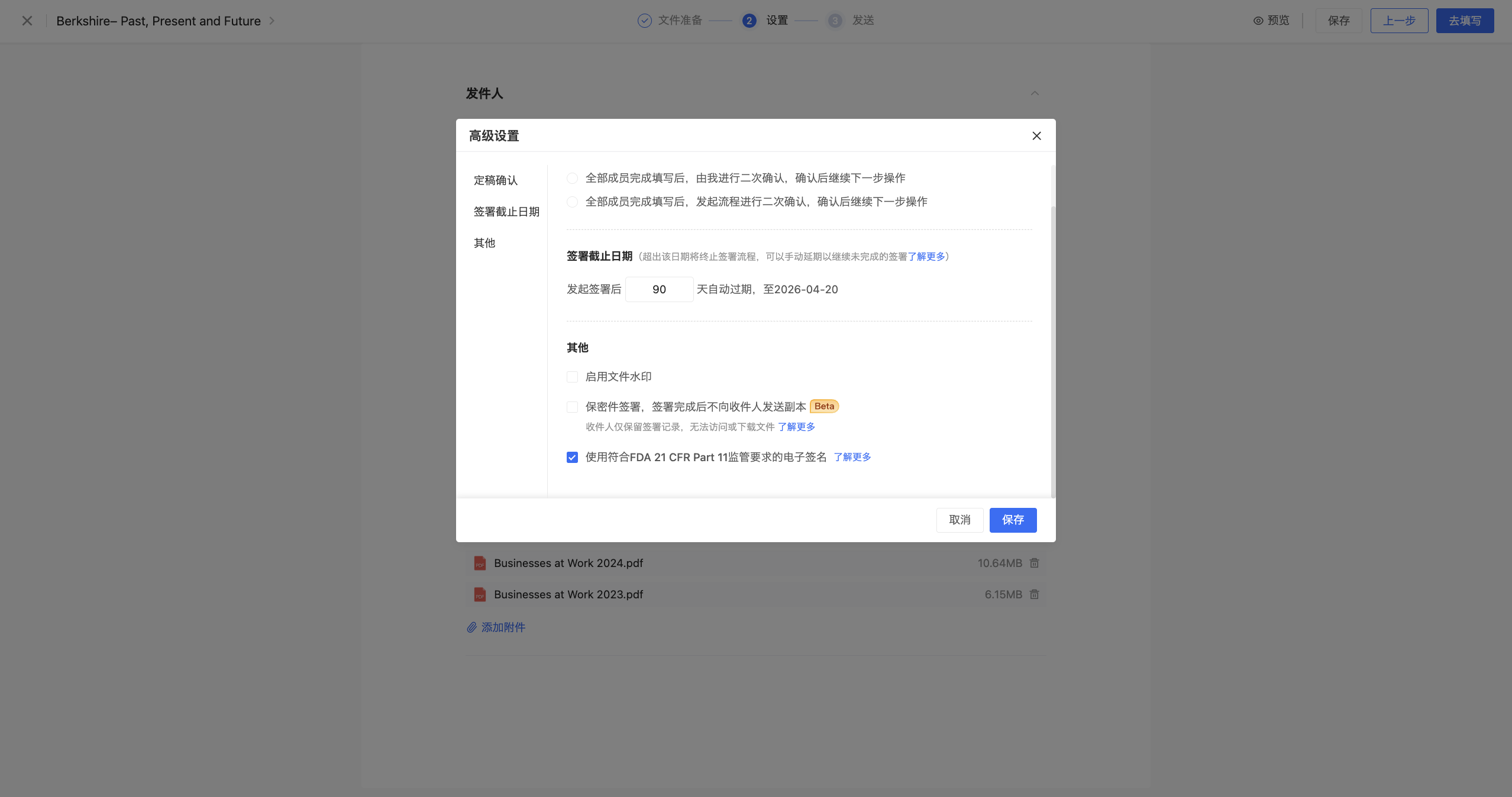
使用符合FDA 21 CFR Part 11监管要求的电子签名
使用符合FDA 21 CFR Part 11监管要求的电子签名
FDA 21 CFR Part 11电子签名合规框架
FDA 21 CFR Part 11电子签名合规框架
如何设置收件人的签署(或确认)顺序 ?
如何设置多人或签 ?
如何设置签署年龄要求 ?
合同签署
合同管理
如何管理企业合同?
如何下载合同?
如何管理企业文件夹?
如何进行签署设置?
如何设置文件夹规则?
模板
归档
审批
证据
智能比对
起草
费用
印章
相对方
自动化助手
企业设置
个人用户使用手册
企微应用端用户操作注意事项
钉钉应用端用户操作注意事项
飞书应用端用户操作注意事项
常见问题
了解电子合同
产品更新日志
问题反馈
问卷调研
使用符合FDA 21 CFR Part 11监管要求的电子签名
最后更新于 2026/02/02 阅读数 761
FDA 21 CFR Part 11是美国食品药品监督管理局(FDA)针对电子记录和电子签名的法规。其目的是确保电子记录和签名的真实性、完整性、可靠性能够等同于纸质记录和手写签名 。Part 11对于电子签名系统提出了多方面要求,主要包括:身份验证、审计追踪、数据完整性与防篡改、系统验证,以及用户权限和访问控制等。

高级设置
👉 更多关联内容:
评价这篇文档
有帮助
没帮助
未能解决您的问题?请联系
在线客服